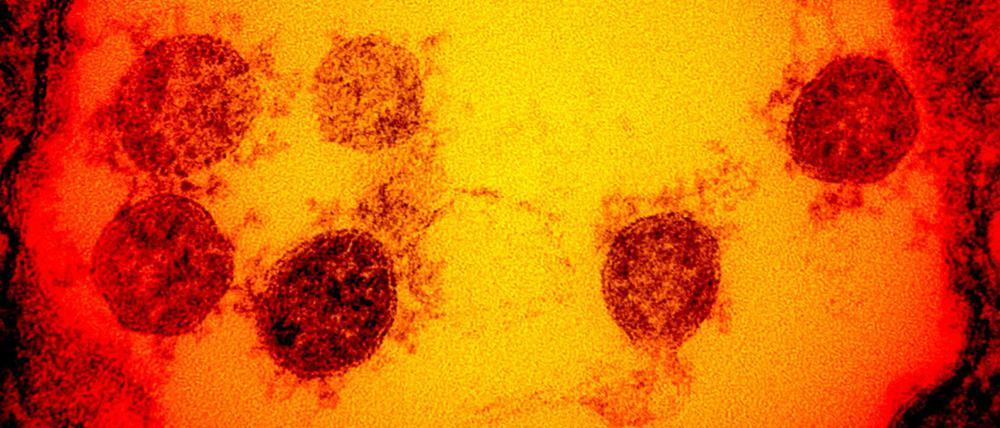
© AFP/National Institute of Allergy and Infectious Diseases(NIH/NIAID)
Gestoppte Covid-19-Studien: Pausen auf dem Weg zu Corona-Arzneien
Unterbrochene Tests, pausierte Studien. Gibt es Probleme bei der Entwicklung von Impfstoffen und Medikamenten gegen Covid-19?
Anfang September musste die Pharmafirma Astra Zeneca Tests ihres Covid-19- Impfstoffs unterbrechen, weil zwei Probanden erkrankten. Am Sonntag wurde bekannt, dass auch Johnson&Johnson eine Impfstoffstudie vorübergehend aussetzt, weil ein Freiwilliger erkrankte. Am Mittwoch nun wurde gemeldet, dass klinische Tests eines monoklonalen Antikörpers gegen das neue Coronavirus, durchgeführt vom Pharmaunternehmen Eli Lilly, vorerst gestoppt wurden.
Eine beunruhigende Häufung von Fehlschlägen? Nein, vorübergehende Stopps klinischer Studien sind durchaus üblich und notwendig. Experten können so überprüfen, ob einzelne Krankheitsfälle von Probanden nur zufällig während der Studie aufgetreten sind oder im Zusammenhang mit dem getesteten Impf- oder Wirkstoff stehen. Allerdings werden solche Pausen in normalen Zeiten kaum in der Öffentlichkeit diskutiert. Jetzt jedoch, da Milliarden Menschen auf Impfstoffe und Arzneien gegen Covid-19 warten, scheint der Nachrichtenwert jeder Studienverzögerung hoch zu sein – und sei sie noch so gewöhnlich.
Das ist wohl auch beim aktuellen Fall so, dem Stopp einer Studie von Eli Lilly, in der einer Gruppe von Patienten der Antikörper LY-CoV555 gegen das Virus gespritzt wurde, der anderen hingegen nur ein Placebo. Den US-amerikanischen National Institutes of Health zufolge wurde die Untersuchung gestoppt, weil das unabhängige Überwachungsgremium, das die Daten ständig sichtet, einen „klaren Unterschied“ zwischen dem Zustand der beiden Patientengruppen erkannt habe. Damit sei eine vor Studienbeginn definierte „Sicherheitsgrenze“ erreicht. Ob damit jedoch gemeint ist, dass es der Patientengruppe, die den Antikörper bekommen hat, erkennbar besser ergeht als der Placebo-Gruppe oder umgekehrt, geht aus dem NIH-Statement nicht hervor.
Die Krankheitsverläufe der bisher in der Studie untersuchten 326 Patienten sollen weiter dokumentiert, aber keine weiteren Patienten in die LY-CoV555-Studie aufgenommen werden. Ende Oktober sollen dann alle Daten gesichtet werden.
Im günstigsten Fall bedeutet der Studienstopp also etwas Positives: dass bereits genug Daten gesammelt wurden, um die Wirksamkeit des Antikörpers zu belegen. Das würde zu den bisherigen Erkenntnissen zu LY-CoV555 passen, denen zufolge der Antikörper die Virusmenge im Nasenrachenraum Infizierter senken und sie vor einer Krankenhauseinweisung bewahren kann. Auch ein ähnlicher Antikörper gegen Sars-CoV-2 der Firma Regeneron, der wohl auch US-Präsident Donald Trump verabreicht wurde, kann wohl ersten Tests zufolge die Virusmenge reduzieren.
Doch es ist auch noch möglich, dass der Stopp der Studie das Gegenteil, das Scheitern von LY-CoV555, bedeutet. Bisher war der Antikörper nur bei Patienten hilfreich, deren Covid-19-Symptome sie noch nicht ins Krankenhaus gezwungen hatten. In der jetzt gestoppten Studie wurden Klinikpatienten behandelt. Sascha Karberg
- showPaywall:
- false
- isSubscriber:
- false
- isPaid:
- showPaywallPiano:
- false